Алкены – определение, номенклатура, получение, свойства
В органической химии углеводород — это органическая молекула, полностью состоящая из водорода и углерода. Углеводороды являются примером гидридов группы 14. Углеводороды бесцветны, гидрофобны, со слабым запахом. Из-за их различной химической структуры трудно делать какие-либо обобщения. Основная часть антропогенных выбросов углеводородов приходится на сжигание ископаемого топлива, которое включает как производство топлива, так и его сжигание. Этилен, изопрен и монотерпены — это полностью природные углеводороды, содержащиеся в выбросах растений.
Что такое Алкены?
Unsaturated hydrocarbons with a double bond between the carbon atoms are known as alkenes. Between carbon-carbon atoms, there is at least one double bond. Alkenes have the generic formula CnH2n. Alkenes are frequently used interchangeably with the term olefin.
The word olefin comes from the Greek phrase olefin gas, which meaning oil-forming gas. Alkenes are extremely reactive chemically due to the presence of double bonds.
Мы все знакомы с насыщенными углеводородами, такими как алканы, но есть еще один класс ненасыщенных углеводородов, присутствующих в сырой нефти, которые более реакционноспособны. Давайте узнаем все, что нужно знать об алкенах, которые представляют собой ненасыщенные углеводороды с по крайней мере одной двойной связью между углерод-углеродными атомами.
Номенклатура алкенов
Алкены имеют общую формулу CnH2n, где n-2, 3, 4, 5 и так далее. Алкены содержат в своих названиях суффикс-ен по системе IUPAC, а префикс определяется числом атомов углерода. Ниже приведены некоторые примеры названий алкенов:
Количество атомов углерода | Формула | название ИЮПАК |
2 | С 2 Н 4 | Этен |
3 | С 3 Н 6 | Пропен |
4 | С 4 Н 8 | Бутен |
5 | С 5 Н 10 | пентен |
6 | С 6 Н 12 | гексен |
7 | С 7 Н 14 | гептен |
8 | С 8 Н 16 | Октен |
9 | С 9 Н 18 | нонен |
10 | С 10 Н 20 | Десен |
Изомерия в алкене
Стереоизомерия и структурная изомерия присутствуют в алкенах.
Стереоизомерия и структурная изомерия присутствуют в алкенах: только одна структура существует в этилене и пропене, в то время как алкены с четырьмя или более атомами углерода демонстрируют как цепную, так и позиционную изомерию.
- Расположение двойной связи не изменяется при цепной изомерии. Цепная изомерия в бутене, например, будет следующей:
- При позиционной изомерии изомеры различаются расположением двойной связи. Два изомера бутена, например, таковы:
Стереоизомерия или геометрическая изомерия. Геометрические изомеры — это изомеры с одинаковой структурной формулой, отличающиеся относительным пространственным расположением атомов или групп атомов вокруг двойной связи. Это явление называется геометрической изомерией. Цис-изомер — это изомер, в котором аналогичная группа атомов находится по одну сторону от двойной связи. С другой стороны, трансизомерия относится к изомеру с сопоставимыми связями на противоположной стороне.
Общие методы получения алкенов.
Алкены получают способами, перечисленными ниже:
- Путем частичного восстановления алкинов. Алкены получают путем гидрирования алкинов в присутствии определенного катализатора, гранулированного древесного угля, который мягко дезактивируется хинолином или соединениями серы.
- Из алкилгалогенидов - алкилгалогениды дегидрируются в алкены при нагревании с сильным основанием, таким как этоксид натрия или концентрированный спиртовой раствор гидроксида калия.
- Из вицинальных галогенидов. Вицинальные галогениды представляют собой дигалогенпроизводные алканов, в которых два атома галогена присутствуют на соседних атомах углерода. При нагревании соответствующих дигалогенидов с цинковой пылью в метаноле или этаноле можно получить алкены.
- Из спиртов . Спирты теряют молекулу воды при нагревании с минеральными кислотами, такими как крепкая серная кислота, с образованием алкенов.
Физические свойства алкенов
- Физическое состояние . Первые три человека представляют собой сухие газы; следующие четырнадцать (C5-C18) представляют собой жидкости, а более высокие - твердые вещества.
- Затенение и запах. За исключением этилена, который имеет чудесный запах, все оставшиеся алкены бесцветны и не имеют запаха.
- Растворимость — алкены нерастворимы в воде, но хорошо растворяются в неполярных растворителях, таких как бензол, бензин, эфир и т. д.
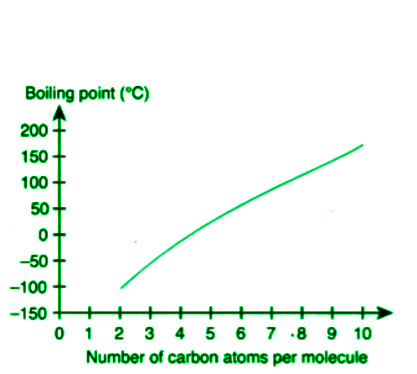
- Точка кипения - Края кипения увеличиваются с увеличением атомной массы. Алкены с прямой цепью имеют более высокие пределы, чем изомерные алкены с удлиненной цепью.
- Все алкены легче воды по плотности. Плотность алкенов растет с увеличением молекулярной массы, пока не будет достигнуто предельное значение 0,8 г/см3.
Химические реакции алкенов
- Добавление водорода. При комнатной температуре алкены быстро присоединяют водород с образованием алканов в присутствии никеля, палладия или платины в качестве катализатора. В качестве примера,
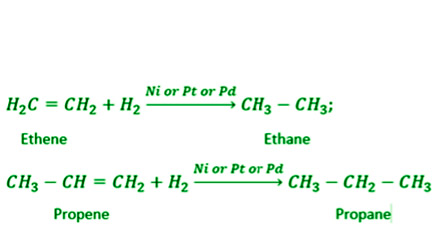
- Добавление галогенов. Производные галогенов образуются, когда алкены реагируют с галогенами в инертном растворе, таком как CCl 4 .
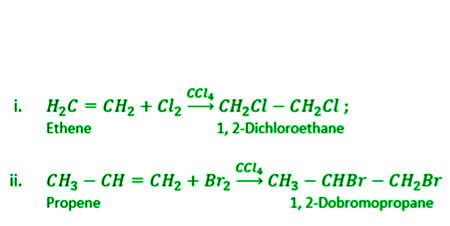
- Добавление галогенидов галогенов. Алкены реагируют с галогенидами галогенов (HCl, HBr, HI) с образованием алкилгалогенидов, которые представляют собой моногалогеналканы.
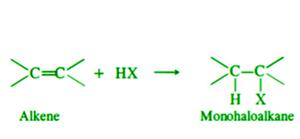
Использование алкенов
- Низшие особи из алкенов используются как энерджайзеры и источники света.
- Алкены и алкены подслоя при полимеризации из многочисленных ценных смесей, таких как полиэтилен, ПВХ, тефлон, орлон и т. д.
- Алкены используются для искусственного созревания органических продуктов.
- Этилен используется при сборке этилового спирта и этиленгликоля.
- Алкены используются для создания агрессивного стука для двигателей.
- Этилен используется в производстве кислородно-этиленового огня для резки и сварки.
Примеры вопросов
Вопрос 1: Какова функция алкенов?
Отвечать:
Alkenes are used to artificially ripen fruits, make anti-knock for vehicle engines, create ethyl alcohol and ethylene glycol, and a variety of other useful chemicals such as polythene, PVC, Teflon, and orlon.
Вопрос 2: Что такое алкен в химии?
Отвечать:
Unsaturated hydrocarbons with a double bond between the carbon atoms are known as alkenes. Between carbon-carbon atoms, there is at least one double bond. Alkenes have the generic formula CnH2n. Alkenes are frequently used interchangeably with the term olefin. The word olefin comes from the Greek phrase olefin gas, which meaning “oil-forming gas.” Alkenes are extremely reactive chemically due to the presence of double bonds.
Вопрос 3: Каковы характеристики алкенов?
Отвечать:
Except for ethene, which has a pleasant odour, all other alkenes are colourless and odourless. Alkenes are insoluble in water but relatively soluble in non-polar solvents such as benzene, petroleum, ether, and others. The boiling point of straight-chain alkenes is greater than that of isomeric branched-chain alkenes.
Вопрос 4: Как мы можем идентифицировать алкены?
Отвечать:
Bromine water can be used to evaluate alkenes. The solution is decolonized by alkenes
Вопрос 5: Каковы два применения алкенов?
Отвечать:
- Alkenes and substituted alkenes are used in the polymerization of several important chemicals such as polythene, PVC, Teflon, and orlon.
- Alkenes are used to make fruits mature artificially.
Вопрос 6: Что такое геометрические изомеры?
Отвечать:
Geometrical isomers are isomers with the same structural formula that differ in the relative spatial arrangement of atoms or groups of atoms around the double bond. Geometrical isomerism is the name given to this occurrence. Cis-isomer is an isomer in which a similar group of atoms is present on the same side of the double bond. Trans-isomerism, on the other hand, refers to an isomer with comparable bonds on the opposite side.